Hallo semua terima kasih sudah berkunjung ke blog saya. Ini adalah tulisan saya yang ke 3.
Kali ini akan membahas tentang ikatan dan unsurkimia.
Oke disimak ya teman-teman.
Unsur Kimia
Unsur kimia adalah suatu spesies atom yang memiliki jumlah proton yang sama dalam inti atomnya (yaitu, nomor atom, atau Z, yang sama). Sebanyak 118 unsur telah diidentifikasi, yang 94 di antaranya terjadi secara alami di bumi. Sedangkan 24 sisanya, merupakan unsur sintetis. Terdapat 80 unsur yang memiliki sekurang-kurangnya satu isotop stabil dan 38 unsur yang merupakan radionuklida yang, seiring berjalannya waktu, meluruh menjadi unsur lain. Besi adalah unsur penyusun bumi paling melimpah (berdasarkan massa), sementara oksigen adalah yang paling melimpah di kerak bumi.
Jari-jari Atom

Jari-jari Ionik

IKATAN KIMIA
Ikatan kimia adalah sebuah proses fisika yang bertanggung jawab dalam interaksi gaya tarik menarik antara dua atom atau molekul yang menyebabkan suatu senyawa diatomik atau poliatomik menjadi stabil.
Ketika dua atom atau ion “berpegangan” dengan sangat erat, dapat dikatan bahwa di antaranya terdapat suatu ikatan kimia. Dalam pembentukannya, yang berperan adalah elektron valensi, yaitu elektron yang berada pada kulit terluar. Untuk memudahkan penggambaran elektron valensi pada atom suatu unsur dan ikatan yang terbentuk dapat digunakan simbol Lewis (simbol titik-elektron Lewis).

Atom-atom cenderung ingin berikatan karena dengan adanya ikatan, energi potensial antara partikel positif dan partikel negatif entah antar ion dengan muatan yang berlawanan ataupun antar inti dengan elektron-elektron di antaranya akan lebih rendah.
Ikatan kimia dibagi menjadi 3 jenis berdasarkan 3 cara kombinasi dari unsur logam dan unsur nonlogam, yakni:
- Logam dengan non logam (ikatan ionik)
- Non logam dengan non logam (ikatan kovalen)
- Logam dengan logam (ikatan logam).
Ikatan ionik (ikatan elektrovalen): “transfer elektron”
Atom logam (energi ionisasi rendah) cenderung melepaskan elektronnya, lalu diterima oleh atom nonlogam (afinitas elektron besar). Dari proses transfer elektron dari atom logam ke atom nonlogam ini akan terbentuk ion positif dan ion negatif dengan konfigurasi elektron gas mulia yang saling tarik menarik dengan gaya elektrostatis yang disebut ikatan ionik. Sebagai contoh, dalam pembentukan senyawa ionik NaCl terjadi transfer elektron dari atom Na ke atom Cl.

Ikatan kovalen: “sharing elektron”
Atom-atom nonlogam cenderung tidak ingin melepaskan elektronnya (energi ionisasi tinggi) dan ingin menarik elektron-elektron dari atom lainnya (afinitas elektron besar) sehingga terdapat satu atau lebih pasangan elektron yang dipakai untuk berbagi bersama. Ikatan kimia yang terbentuk dari sharing elektron terlokalisasi antara atom ini disebut ikatan kovalen. Sebagai contoh, 2 atom H berikatan kovalen membentuk molekul H2 dan 2 atom Cl berikatan kovalen membentuk molekul Cl2.

Struktur Lewis untuk senyawa kovalen dapat digambarkan dengan setiap pasangan elektron ikatan (PEI) digambarkan sebagai satu garis dan pasangan elektron bebas (PEB) digambarkan sebagai titik-titik. Berikut struktur Lewis untuk beberapa senyawa kovalen.

Ikatan kovalen dengan berbagi satu pasangan elektron disebut sebagai ikatan kovalen tunggal (ikatan tunggal). Ikatan kovalen dengan berbagi dua pasangan elektron disebut ikatan rangkap dua, contohnya CO2. Ikatan kovalen dengan berbagi tiga pasangan elektron disebut ikatan rangkap tiga, contohnya N2.

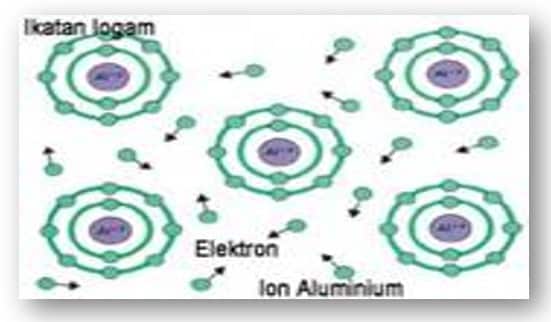
Ikatan Logam
Mantap
BalasHapussangat membantu, tq
BalasHapusTerimakasih yaa,threadnya sangat membantuuu😊
BalasHapusbagus dan sangat bermanfaat kak
BalasHapusKomentar ini telah dihapus oleh pengarang.
BalasHapusThanks, sangat membantu dan bermanfaat
BalasHapusSangat bermanfaat. Terimakasih
BalasHapusSangat membantu dan bermanfaat. Semangat menulis blog tentang materi yang lain ya kak.
BalasHapusThanks sgt bermanfaat 👍
BalasHapusSangat membantu
BalasHapusMantap warbiyasaah
BalasHapuspembahasannya bagus :)
BalasHapusMantap kak
BalasHapusbaguss
BalasHapusSangat bermanfaat kak, mkasih
BalasHapus👍👍👍
BalasHapusSangat bermanfaat. terima kasih :)
BalasHapusBagus kak
BalasHapusNice blognya kak
BalasHapusSangat bermanfaat
BalasHapusMakasih kak sangat bermanfaat!
BalasHapus